グリーティング
酵素をはじめとするタンパク質は、生体内の反応を触媒するなど生物にとって欠くことのできない重要な分子です。その大きさはナノメートルのオーダー(100万分の1 mm)にも関わらず、見事な立体構造をもち、1回の反応にたったマイクロ秒からミリ秒しかかからない、精密分子機械です。タンパク質は、われわれが日常意識しない大きさ、時間スケールで稼働しています。一方で、この分子はさほど安定ではなく、少し条件がかわると壊れてしまうような儚さももちあわせています。私は学生時代から精密分子機械であるタンパク質の構造や働く仕組みに魅せられて研究・実験をしています。昨今はとくに、微生物のタンパク質・酵素を対象として、遺伝子工学、種々の物理化学的手法を用いて、どんなふうに立体構造を作りあげるのか、どのような仕組みで作動するのかについて研究しています。微生物が産生するタンク質は、彼らの生育環境を反映して、多芸なもの(100度以上の高温でも働くタンパク質など)が多く、さらに、これらは人類社会にとっても有用なもの多くあり、好個の研究対象です。をかしな微生物がつくるタンパク質の研究を続け、有用なタンパク質の開発などで人類社会に貢献したいと考えています。
研究分野・テーマ
1. 基質をスライドさせて連続反応をおこなう酵素の作動機構の解明
通常の酵素は一度反応すると、反応相手(基質)と離れて、また別の基質を探します。他方、少数ですが、基質を捉えたままスライドさせて次々に連続反応する効率のよい酵素もあります。私たちは、キチンという多糖ポリマーを連続分解するキチナーゼを対象として、どのような仕組みで連続分解を可能にしているのかに迫ろうといています。このテーマは私が所属する研究室(応用微生物学研究室)で続けられてきた研究で、新潟大学赴任後に参加しました。細菌由来のキチナーゼを研究対象としていますが、同じ細菌が作るキチナーゼでも、連続分解するものとそうでないものがあり、しかも両者の姿は似ています。そのなかで、なにか連続分解のキーファクターになっているのか、なにが反応駆動力になっているのかを明らかにしようとしています。
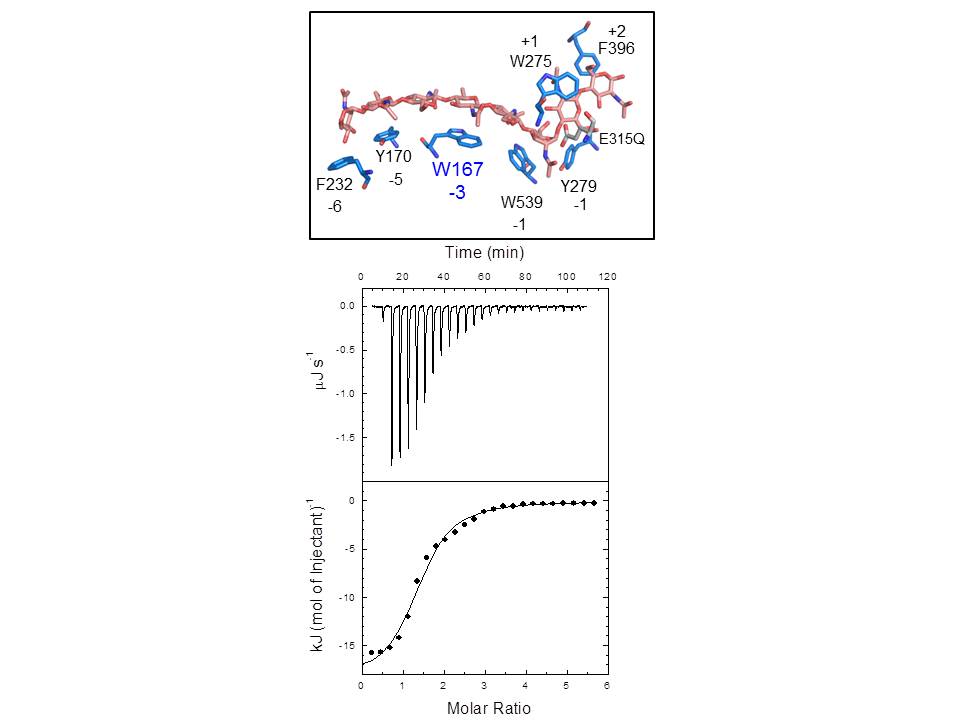 連続反応キチナーゼの構造と基質結合の熱測定
連続反応キチナーゼの構造と基質結合の熱測定
2.タンパク質の折りたたみ・安定性に関する研究
黒コウジカビがつくるグルコアミラーゼ(デンプンを分解する酵素)のデンプン結合ドメインなどの小型球状タンパク質を対象として、タンパク質の構造形成過程(折たたみ過程)と構造安定性について研究しています。タンパク質分子はもともとアミノ酸が数珠状に連なったひも状分子として生成されますが、その後折りたたまれ、ひとりでに緻密な立体構造を作ります。折りたたみ過程や安定性を調べるには、タンパク質分子を壊して(変性させて)影響を調べたり、壊れていく過程や巻き戻る過程を解析します。これにより、どんな仕組みでタンパク質分子の立体構造が維持されているのか、そのような仕組みで折りたたまれて見事立体構造を形成するのかを明らかにしようとしています。
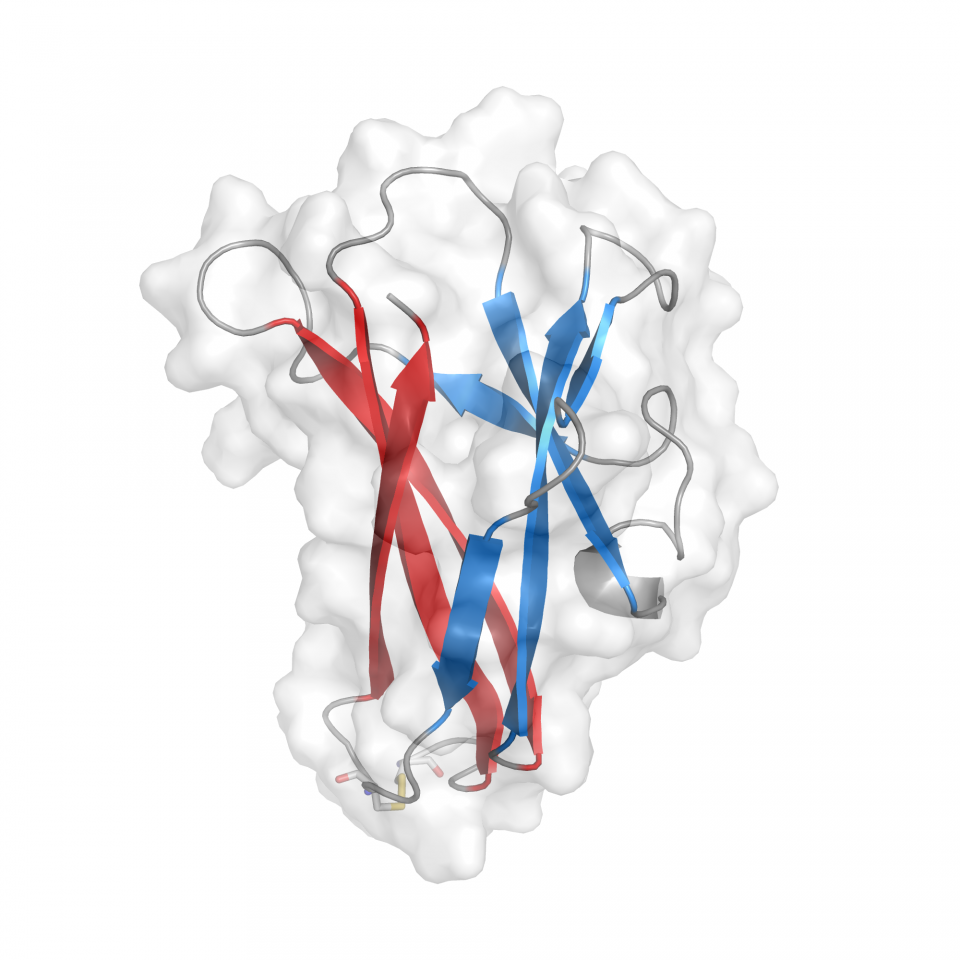 デンプン結合ドメインの立体構造
デンプン結合ドメインの立体構造
研究業績・略歴
アルバム
 相棒の熱量計とパシャリ
相棒の熱量計とパシャリ 研究室学生によるオープンキャンパスでの展示
研究室学生によるオープンキャンパスでの展示 卒業祝賀会にて
卒業祝賀会にて
リンク






















